На заметку
Основные разделы сайта
- Физическая химия
- Органическая химия
- Неорганическая химия
- История химии
- Cтроение атома и химическая связь
- Газы, жидкости и твердые вещества, стехиометрия, энергетика
- Фазовые равновесия, химическое равновесие, ионы, химическая кинетика
- Электрохимия
- Теория вакуумных систем
- Теория космического вакуума ч.1
- Теория космического вакуума ч.2
- Реакции в порошковых смесях
- Новости сайта
- Контакты
Аналитическая химия на примерах
Физическая химия на примерах
Разное
Методы практической химии
Диаграммы состояния бинарных систем
- Обзор
- Ac-B . . . Al-Sr
- Al-Tl . . . Au-Pr
- Au-Pt . . . B-Zr
- B-Zr . . . Be-Zr
- Bi-Br . . . Bi-Zr
- Bk-Mo . .Ca-Zn
- Cd-Ce . . Ce-Zr
- Cf-Mo . . Cr-Zr
- Cs-F . . . Dy-Zr
- Er-Fe . . . F-Yb
- Fe-Ga . . Ga-Zr
- Gd-Ge . . .Ge-Zr
- H-Hf . . . Hg-Zr
- Ho-I . . . Ir-Zr
- K-li . . . Lu-Zr
- Md-Mo . . Mo-Zr
- N-Nb . . . Nd-Zr
- Ni-O . . . Pb-Zr
- Pd-Pt . . . Pu-Zr
- Rb-S . . . Sc-Zr
- Se-Sn . . Tl-Zn
- Tm-V . . . Zn-Zr
Видеотека


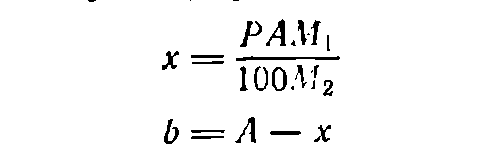 (5)
(5)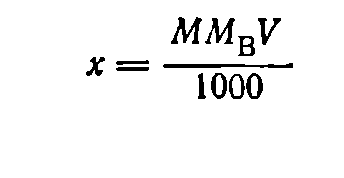 (7)
(7) (10)
(10)