Атомные радиусы
Определение атомных радиусов также связано с некоторыми проблемами. Во-первых, атом не является сферой со строго определенными поверхностью и радиусом. Напомним, что атом представляет собой ядро, окруженное облаком электронов. Вероятность обнаружения электрона по мере удаления от ядра постепенно возрастает до некоторого максимума, а затем постепенно уменьшается, но становится равной нулю только на бесконечно большом расстоянии. Во-вторых, если мы все же выберем некоторое условие для определения радиуса, такой радиус все равно нельзя будет измерить экспериментально.
Эксперимент позволяет определять только межъядерные расстояния, другими словами-длины связей (и то с определенными оговорками, приведенными в подписи к рис. 2.21). Для их определения используется рентгеноструктурный анализ или метод электронографии (основанный на дифракции электронов). Радиус атома полагают равным половине наименьшего межъядерного расстояния между одинаковыми атомами.
Вандерваальсовы радиусы. Для несвязанных между собой атомов половина наименьшего межъядерного расстояния называется вандерваальсовым радиусом. Это определение поясняет рис. 2.22.
Рис. 2.21. Длина связи. Вследствие того что молекулы непрерывно колеблются, межъядерное расстояние, или длина связи, не имеет фиксированного значения. Этот рисунок схематически изображает линейное колебание простой двухатомной молекулы. Колебания не позволяют определить длину связи просто как расстояние между центрами двух связанных атомов. Более точное определение выглядит так: длина связи это расстояние между связанными атомами, измеренное между центрами масс двух атомов и соответствующее минимуму энергии связи. Минимум энергии показан на кривой Морзе (см. рис. 2.1).


Таблица 2.6. Плотности аллотропов углерода и серы Таблица 2.7. Длина связей углерод - углерод
Ковалентные радиусы. Ковалентный радиус определяется как половина межъядерного расстояния (длины связи) между двумя одинаковыми атомами, связанными друг с другом ковалентной связью (рис. 2.22, б). В качестве примера возьмем молекулу хлора Cl2, длина связи в которой составляет 0,1988 нм. Ковалентный радиус хлора полагается равным 0,0944 нм.
Зная ковалентный радиус атома одного элемента, можно вычислить ковалентный радиус атома другого элемента. Например, экспериментально установленное значение длины связи С—Cl в CH3Cl равно 0,1767 нм. Вычитая из этого значения ковалентный радиус хлора (0,0994 нм), находим, что ковалентный радиус углерода равен 0,0773 нм. Такой метод вычисления основан на принципе аддитивности, согласно которому атомные радиусы подчиняются простому закону сложения. Таким образом, длина связи С—Cl представляет собой сумму ковалентных радиусов углерода и хлора. Принцип аддитивности применим только к простым ковалентным связям. Двойные и тройные ковалентные связи имеют меньшую длину (табл. 2.7).
Длина простой ковалентной связи зависит еще от ее окружения в молекуле. Например, длина связи С—H изменяется от 0,1070 нм у тризамещенного атома углерода до 0,115 нм в соединении CH3CN.
Металлические радиусы. Металлический радиус полагается равным половине межъядерного расстояния между соседними ионами в кристаллической решетке металла (рис. 2.22, в). Термин атомный радиус обычно относится к ковалентному радиусу атомов неметаллических элементов, а термин металлический радиус~к атомам металлических элементов.
Ионные радиусы. Ионный радиус-это одна из двух частей межъядерного расстояния между соседними одноатомными (простыми) ионами в кристаллическом ионном соединении (соли). Определение ионного радиуса тоже сопряжено с немалыми проблемами, поскольку экспериментально измеряют межионные расстояния, а не сами ионные радиусы. Межионные расстояния зависят от упаковки ионов в кристаллической решетке. На рис. 2.23 показаны три возможных способа упаковки ионов в кристаллической решетке. К сожалению, экспериментально измеренные межионные расстояния
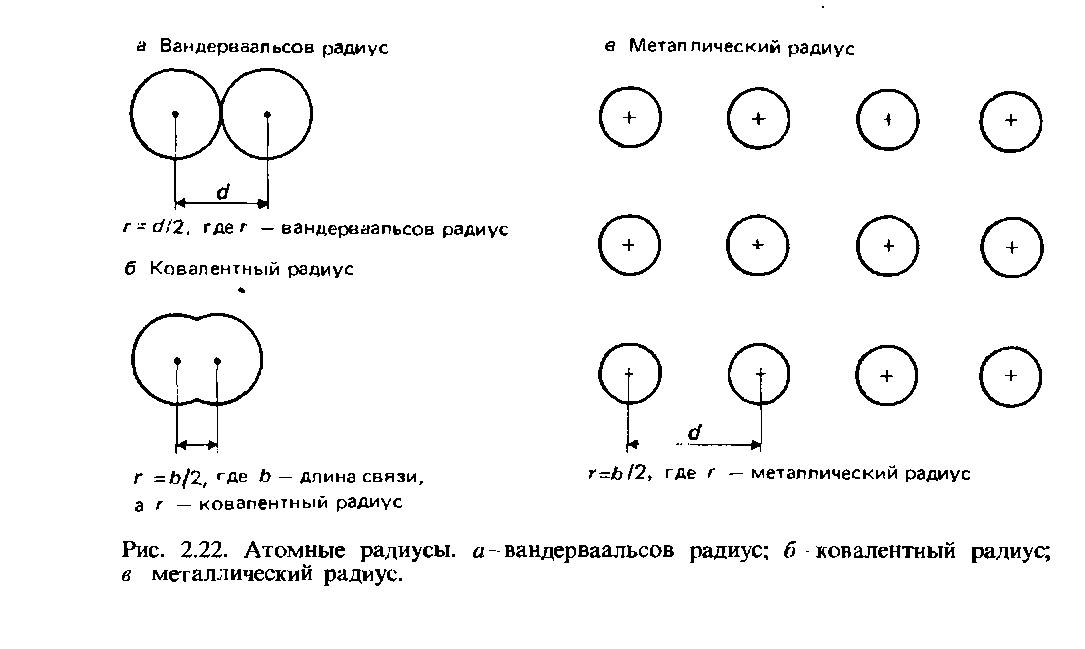
Рис. 2.23. Ионные радиусы, с-анионы соприкасаются друг с другом, но катионы не соприкасаются с анионами; б-катионы соприкасаются с анионами, но анионы не соприкасаются друг с другом; в условно принятое расположение ионов, при котором катионы соприкасаются с анионами и анионы соприкасаются друг с другом. Расстояние а определяется экспериментально. Оно принимается за удвоенный радиус аниона. Это позволяет вычислить межионное расстояние b, представляющее собой сумму радиусов аниона и катиона. Зная межионное расстояние Ь, можно вычислить радиус катиона.
не позволяют судить о том, какой из этих трех способов упаковки действительно осуществляется в каждом конкретном случае. Проблема заключается в том, чтобы найти пропорцию, в которой следует разделить межионное расстояние на две части, соответствующие радиусам двух ионов, другими словами, решить, где же на самом деле кончается один ион и где начинается другой. Как показывает, например, рис. 2.12, этот вопрос не позволяют решить и карты электронной плотности солей. Для преодоления указанной трудности обычно предполагают, что: 1) межионное расстояние представляет собой сумму двух ионных радиусов, 2) ионы имеют сферическую форму и 3) соседние сферы соприкасаются друг с другом. Последнее предположение соответствует способу упаковки ионов, изображенному на рис. 2.23, е. Если известен один ионный радиус, другие ионные радиусы можно вычислить на основании принципа аддитивности.
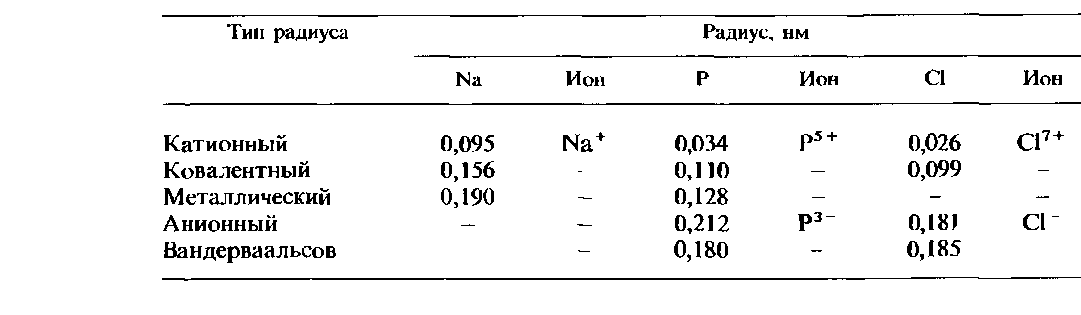
Сопоставление радиусов различных типов. В табл. 2.8 указаны значения радиусов различных типов для трех элементов 3-го периода. Нетрудно видеть, что самые большие значения принадлежат анионным и вандерваальсовым радиусам. На рис. 11.9 сопоставлены размеры ионов и атомов для всех элементов 3-го периода, за исключением аргона. Размеры атомов определяются их ковалентными радиусами. Следует обратить внимание на то, что катионы имеют меньшие размеры, чем атомы, а анионы - большие размеры, чем атомы этих же элементов. Для каждого элемента из всех типов радиусов наименьшее значение всегда принадлежит катионному радиусу.
Таблица 2.8. Сопоставление атомных радиусов различных типов

Экспериментальное определение. Для определения формы простых молекул и многоатомных ионов, а точнее - длин связей и валентных углов (углов между связями), используются разнообразные экспериментальные методы. К ним относятся микроволновая спектроскопия, а также методы изучения дифракции рентгеновских лучей (рентгеноструктурный анализ), нейтронов (нейтронография) или электронов (электронография). В следующей главе подробно рассказывается о том, каким образом с помощью дифракции рентгеновских лучей можно определять кристаллическую структуру. Однако для определения формы простых молекул в газовой фазе обычно используется электронография (метод изучения дифракции электронов). Этот метод основан на использовании волновых свойств электронов. Пучок электронов пропускают сквозь образец исследуемого газа. Молекулы газа рассеивают электроны, и в результате возникает дифракционная картина. Анализируя ее, можно определить длины связей и валентные углы в молекулах. Этот метод аналогичен используемому при анализе дифракционной картины, образуемой при рассеянии рентгеновских лучей.
Оглавление:
