Ионные и ковалентные соединения
Соединения двух элементов, расположенных в противоположных концах одного (или разных) периодов, имеют преимущественно ионный характер связи, но по мере сближения элементов в пределах периода ионный характер их соединений уменьшается, а ковалентный характер-увеличивается. В большинстве случаев нельзя сказать, что соединение является полностью (или чисто) ионным либо полностью (или чисто) ковалентным. Однако можно утверждать, что некоторые соединения являются преимущественно ионными, а другие соединения преимущественно ковалентными.
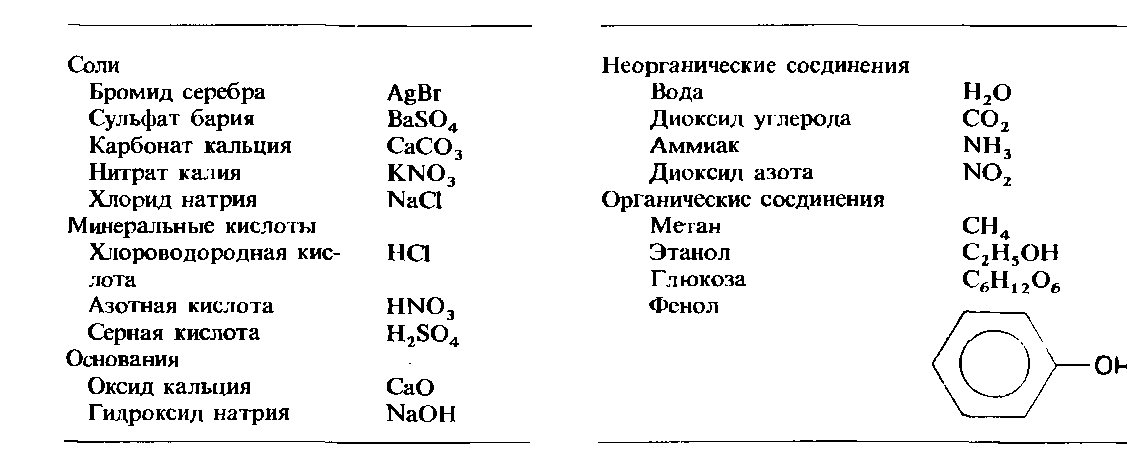
Хорошими примерами сказанного являются хлориды и оксиды. Хлориды и оксиды элементов, расположенных в левой части периодической таблицы, как правило, имеют преимущественно ионный характер, а хлориды и оксиды элементов из правой части периодической таблицы являются преимущественно ковалентными соединениями. Хлориды и оксиды промежуточных элементов имеют смешанный характер связи-ионный с большой степенью ковалентности. В табл. 2.3 и 2.4 приведены примеры соединений, которые обычно рассматриваются как ионные и соответственно ковалентные.
Таблица 2.3. Примеры ионных соединений Таблица 2.4. Примеры ковалентных соединений
Электроны, участвующие в образовании металлической связи, являются внешними, или валентными, электронами атомов металла. Эти валентные электроны уже не принадлежат каждый определенному атому металла, а делокализованы между положительными ионами. Делокализованные внутри металла электроны не располагаются парами на связывающих орбиталях между соседними ионами, а находятся на гигантских орбиталях, которые простираются по всей кристаллической решетке. Эти орбитали футшируются по энергии в отдельные зоны. В пределах одной зоны имеется множество орбиталей с разными энергетическими уровнями; соседние энергетические уровни имеют почти одинаковую энергию. Валентные электроны металлов, принадлежащих к I группе периодической системы, частично заполняют самую низкую энергетическую зону. Она называется s-зоной. Металлы II группы имеют полностью заполненную s-зону. После того как одна зона заполнена, электроны начинают заполнять следующую, более высокую по энергии зону (рис. 2.14).
Оглавление:
